今天是:
![]()
![]()
近期,足球比分直播生物工程学院赵群教授和浙江工业大学杨云芳教授、赫罗纳大学Marc Garcia-Borràs教授、约翰霍普金斯大学Xiongyi Huang教授在金属酶催化新功能拓展方面取得重要进展,研究成果“Engineering non-haem iron enzymes for enantioselective C(sp3)–F bond formation via radical fluorine transfer.”正式发表于《Nature Synthesis》杂志。
将氟原子或含氟片段引入药物分子,能够有效地改变药物分子的pKa、脂溶性、代谢稳定性以及渗透性,影响药物分子的吸收、分布和代谢。因此,向药物分子中引入“氟”已经成为药物开发中非常重要的一部分,逐步成为药物筛选的一种常用手段。2021年美国FDA批准的小分子药物中,30%都是有机氟化合物。目前,超过25%的药物都是有机氟化合物。制药工业对含氟化合物的高需求极大地推动了有机氟化学的发展,越来越多的化学合成方法被应用于制备含氟分子,药物开发中的含氟分子数量剧增。
与之相反,自然界中含氟分子的数量却十分有限。到目前为止,人们仅发现约30种天然有机氟化合物,但是同为卤素家族的天然有机氯化合物和有机溴化合物有近2000种已被发现。导致自然界中有机氟化合物稀缺的一个重要原因是酶促碳–氟键形成机制的单一性,目前唯一已知能够在生物合成途径中催化C–F键形成的酶是氟化酶(Fluorinase),它能够催化氟负离子亲核进攻S-腺苷甲硫氨酸(SAM)产生5'-氟脱氧腺苷(5'-FDA)。但是,自然界进化产生的氯化酶和溴化酶可以利用多种反应机制来构建碳–卤键,如:经历次氯酸根中间体的亲电卤代机制、经历铁氧中间体的自由基卤代机制以及亲核卤代机制(图1)。
目前,通过酶促反应合成有机氟化合物的研究,主要集中在拓展氟化酶的底物范围以及将含氟砌块引入代谢途径这两大策略,尽管已经取得了一定进展,但是酶催化C–F键形成的发展仍显不足。如何建立新的生物催化机制来构建C–F键仍然是酶催化领域中颇具挑战性的科学难题。鉴于此,研究团队近日共同报道了基于新催化机制的酶促不对称氟化反应,首次将自由基氟原子转移机制引入到单一金属酶催化体系,实现了高立体选择性的氟转移过程(图2)。
本文研究团队建立了一种能够介导不对称氟原子转移反应的酶催化体系。这项工作证明非血红素铁酶中的铁–氟中间体能够与碳自由基反应生成碳–氟键,这也预示着其它的非血红素铁酶有望参与自由基型的氟转移反应,能够用于开发非天然途径的氟化反应。该工作为非血红素铁酶的进一步工程化改造提供了借鉴,也为酶促氟化反应提供了新的思路。
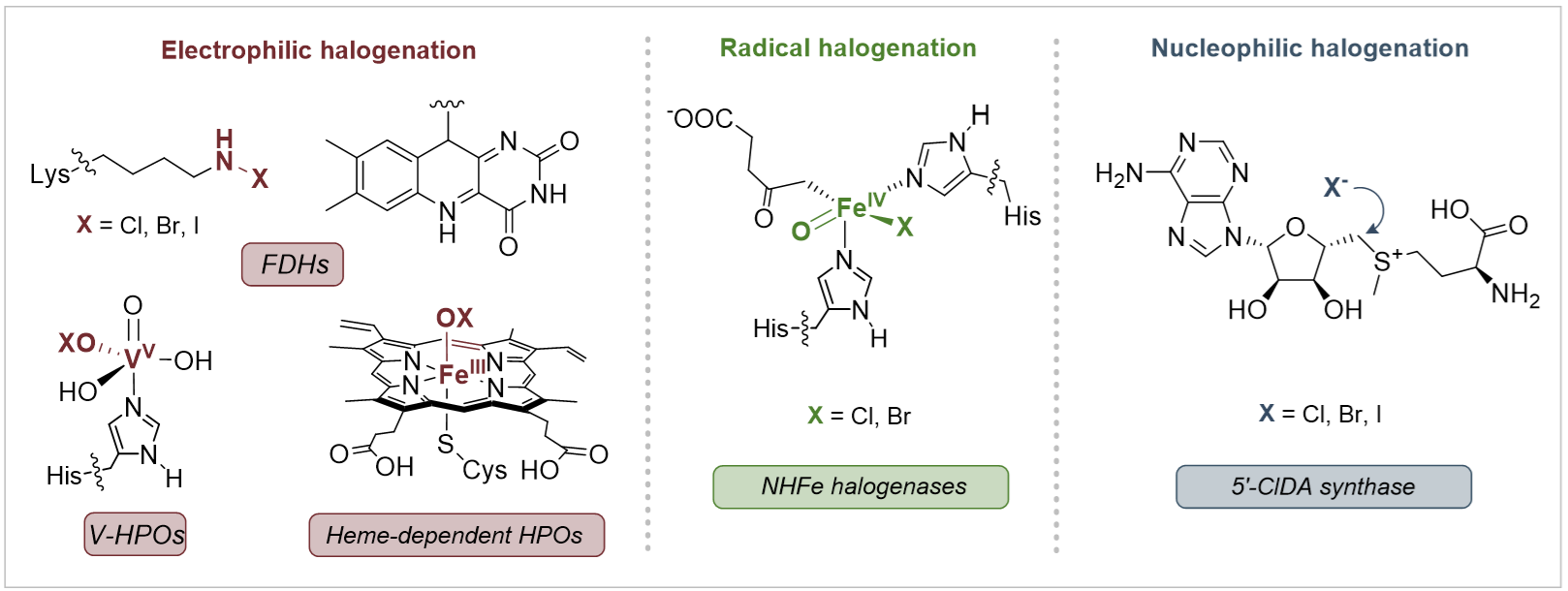
图1:卤化酶催化机制
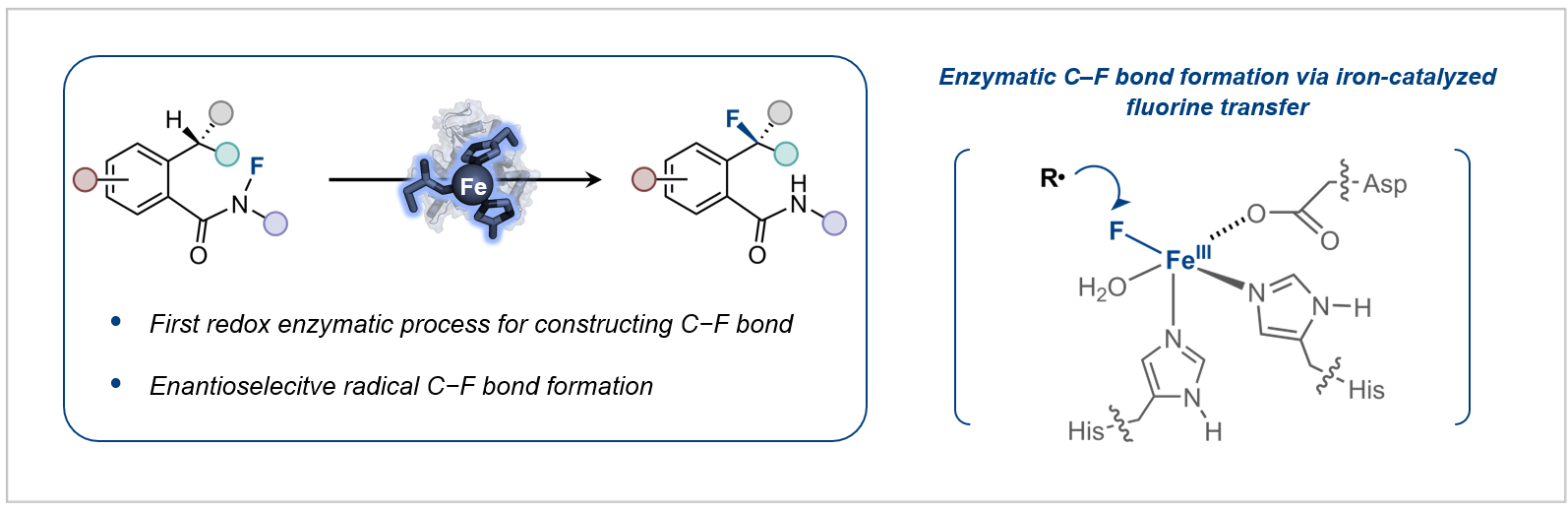
图2:酶催化不对称氟转移反应
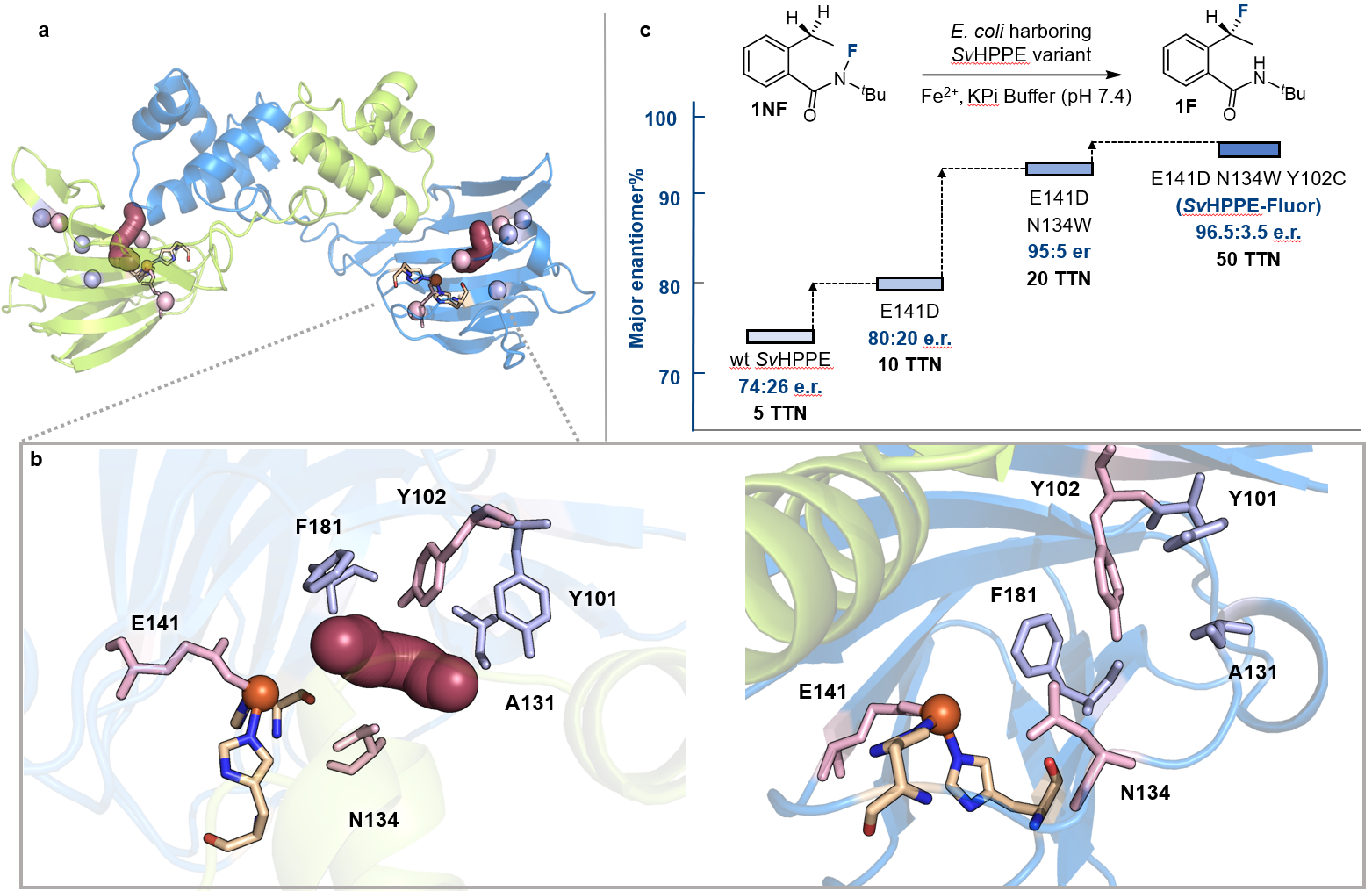
图3:酶定向进化对反应进行优化

图4:酶促反应的底物范围
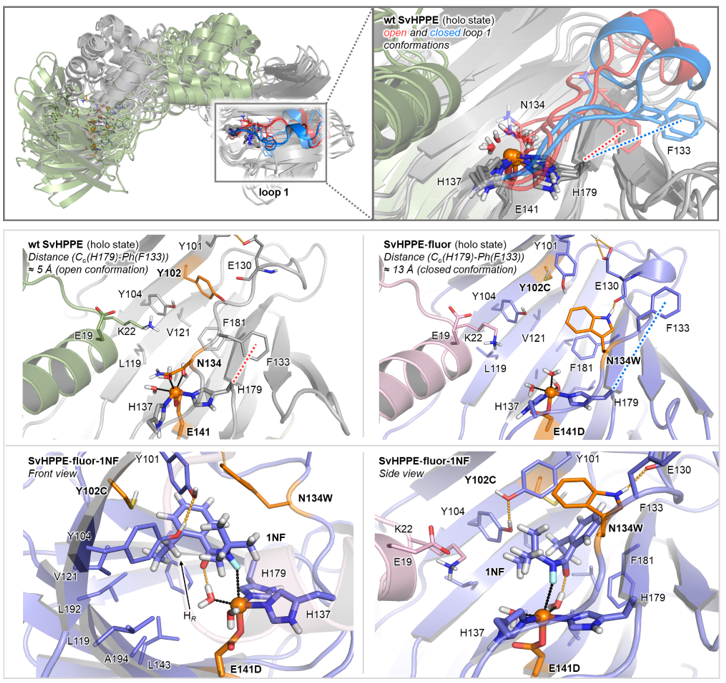
图5:分子动力学模拟(MD)

地址:江苏省无锡市蠡湖大道1800号
邮编:214122
联系电话:0510-85326517
服务邮箱:xck@jiangnan.edu.cn
